
2025-09-18 19:32:33
基因療法制造商面臨的挑戰與抗體療法剛出現時單克隆抗體制造商面臨的挑戰相似。例如,在生產、儲存和處理過程中,單克隆抗體也會受到低滴度、產品和工藝相關雜質和降解的挑戰。盡管與重組單克隆抗體相比,單劑量AAV產品與工藝相關雜質相關的風險可能更低(取決于雜質的類型、劑量和給藥途徑),但這也不能忽視。由于這些相似性,制藥商、化學品和輔料供應商有機會進行合作,并開發創新的解決方案,以實現穩健和成本效益高的AAV產品生產。高鹽能夠抑制AAV病毒載體聚集,提高AAV病毒載體產量。浙江倍篤生物高鹽核酸酶聯系方式
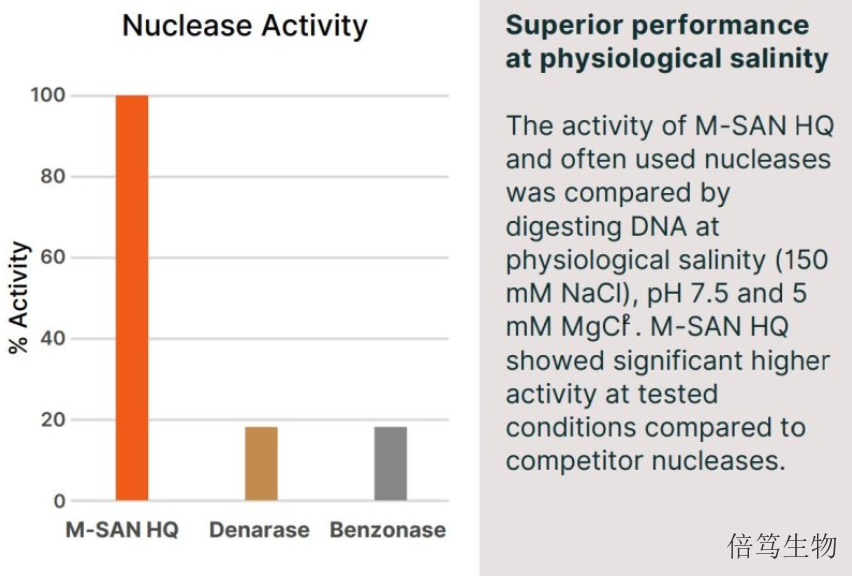
目前基因藥物領域常用的病毒載體有腺病毒、慢病毒、重組腺相關病毒(rAAV)以及逆轉錄病du等,其中AAV因其免疫原性極低、**性高、宿主細胞范圍廣、擴散能力強、表達穩定以及特異性強等優勢脫穎而出。據NIH統計,已有超過200個正在進行或已完成的基因藥物臨床試驗使用rAAV載體。盡管rAAV基因藥物已顯示出巨大的前景,但是強大、穩健而且可放大的基因載體生產制造工藝一直是CGT行業的痛點。目前rAAV生產平臺主要有三種:三質粒瞬轉體系(TransientTransfection, TT)、桿狀病毒表達載體體系(Baculovirusexpression vector,BEV)和包裝細胞體系(Packaging/Producercell line,PCL)。 江蘇70950-150高鹽核酸酶價格高鹽濃度下,宿主DNA與蛋白質能夠更高效解離,從而更容易被降解。
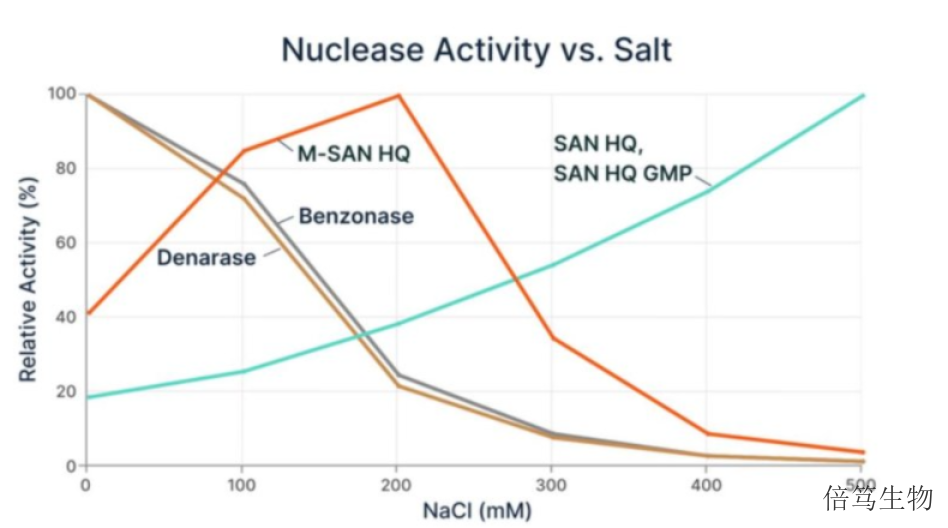
ArcticZymes Technologies成立于20世紀80年代后期,總部位于挪威北部的特羅姆瑟(Troms?)。在生物制品生產,如AAV載體及腺病毒載體疫苗生產中,宿主細胞DNA殘留是關鍵質量參數之一,高鹽濃度下,宿主DNA與蛋白質能夠更高效解離,從而更容易被降解。ArcticZymes廠家管控整個供應鏈及生產流程,協助客戶進行文件審計及現場審計。1.高鹽濃度下,宿主DNA與蛋白質能夠更高效解離,從而更容易被降解。在AAV生產過程中鹽濃度是純化工藝的重要參數之一,高鹽濃度能夠減少目標產物聚集、增加目標產物溶解度及提高目標產物產量。
經過多年的經驗積累及市場積淀,倍篤生物已組合多條不同產品線,分別滿足體外診斷、organoid及干細胞、細胞基因藥物等領域的需求。其中,細胞基因藥物領域產品線包含SAN HQ高鹽核酸酶及M-SAN HQ中鹽核酸酶、泊洛沙姆P 188 Bio、GMP級MSC/PSC培養基、GMP級膠原酶、AAV滴度檢測產品、工藝雜質及外源污染物殘留檢測產品、AAV中和抗體蛋白酶等;相關品牌有挪威ArcticZymes Technologies、德國BASF、德國Sartorius、德國Nordmark、瑞典Genovis、中國君研生物等。SAN HQ高鹽核酸酶是用Pichia pastoris表達的重組非特異性內切核酸酶。
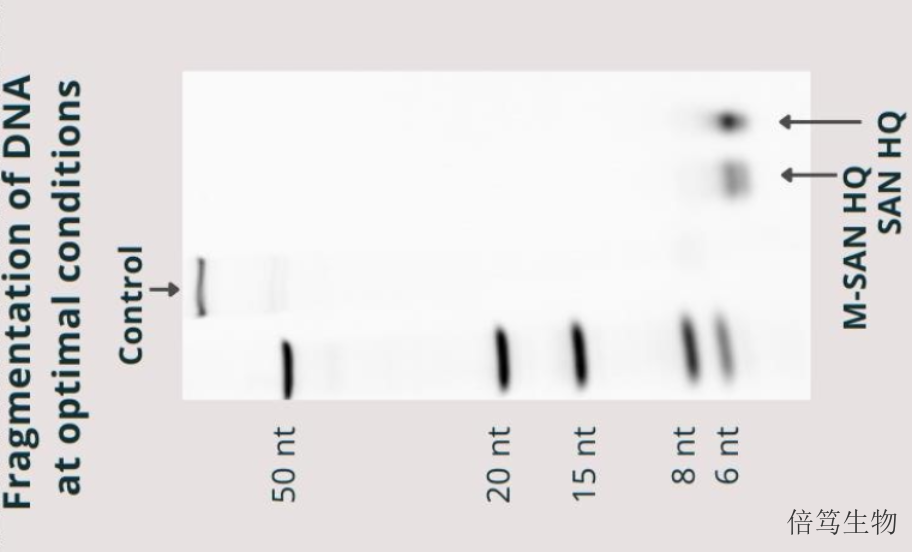
ArcticZymes廠家對鹽活性核酸酶系列產品(Salt Active Nucleases,SANs)的生產及質控,在符合ISO13485:2016體系基礎上,增加了cGMP質控標準,如microbes、endotoxin、蛋白酶等,符合USP-EP要求。廠家提供HQ級別和GMP級別的SAN HQ高鹽核酸酶和M-SAN HQ中鹽核酸酶,從成本角度分別滿足臨床前和早期臨床階段、商業化大規模生產階段的需求;且GMP級SAN HQ高鹽核酸酶已完成在FDA的藥物主文件(Drug Master File, DMF)申報備案,助力加快藥物申報流程。東臺高鹽核酸酶服務哪家好呢,歡迎咨詢上海倍篤生物 。浙江70921-150高鹽核酸酶量大優惠
無錫高鹽核酸酶售后服務哪家好呢,歡迎咨詢上海倍篤生物 。浙江倍篤生物高鹽核酸酶聯系方式
通過三質粒瞬轉體系生產病毒載體,會引入宿主細胞DNA殘留(HCD)、蛋白殘留(HCP)、工藝雜質(如antibiotics、核酸酶等外源物質)等污染,存在潛在的致瘤性和免疫原性等風險。藥品監管機構一般允許生物制品中存在10ng/dose以下的殘留DNA。此外,根據雜質來源、工藝以及產品類型不同,也會對HCD限度做不同要求。為了達到這個要求,一般通過核酸酶處理和色譜聯用的方法。一般在細胞培養液裂解/收獲、澄清收獲及超濾濃縮等環節加入核酸酶處理,需要工藝摸索來確認處理方式。浙江倍篤生物高鹽核酸酶聯系方式